| 文水县食品药品监督管理局权力和责任清单 | |||||||||
| 权力清单 | 责任清单 | 备注 | |||||||
| 职权类别 | 职权编码 | 职权名称 | 职权依据 | 责任事项 | 追责情形 | 追责依据 | 追责形式 | ||
| 项目 | 子项 | ||||||||
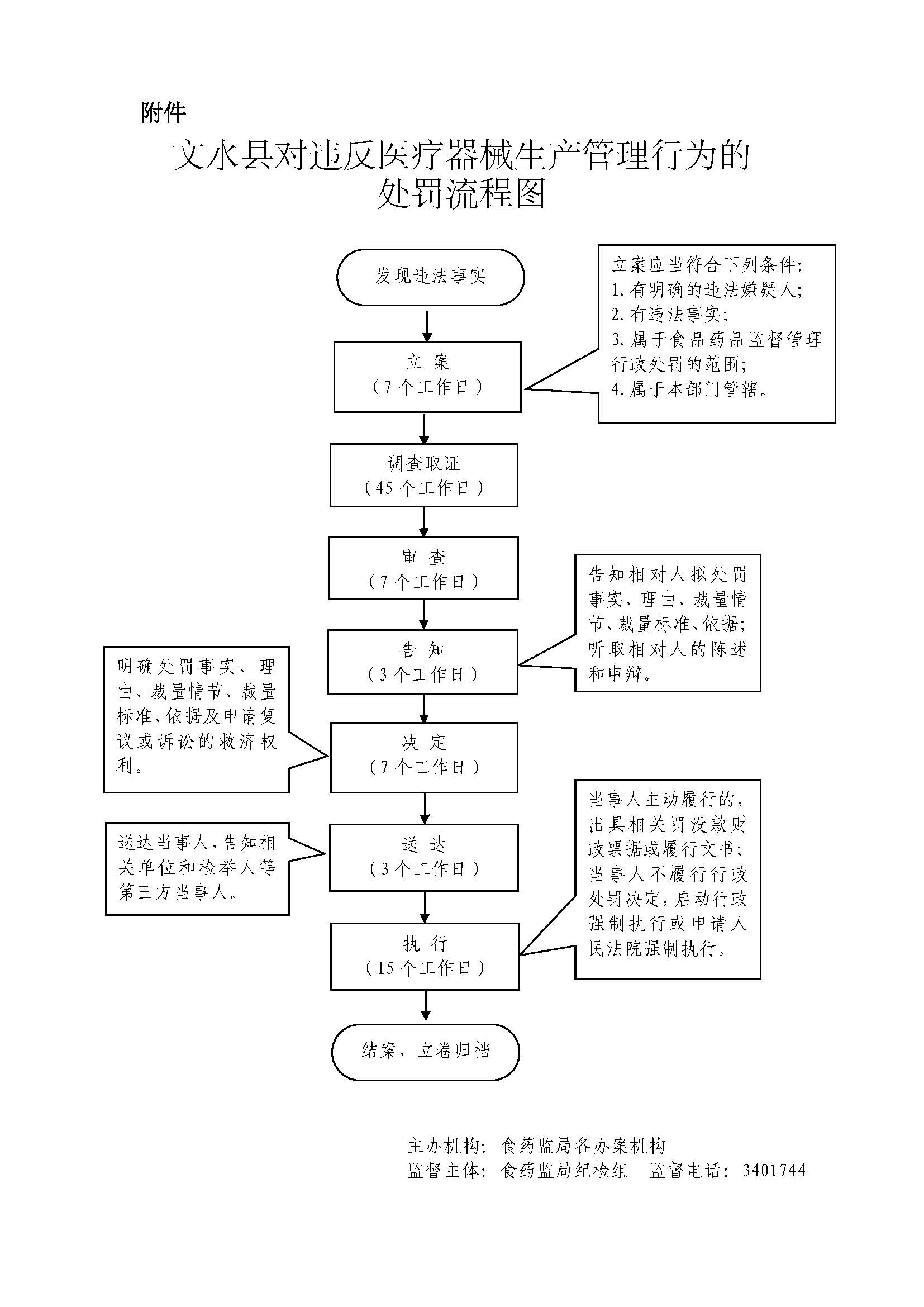
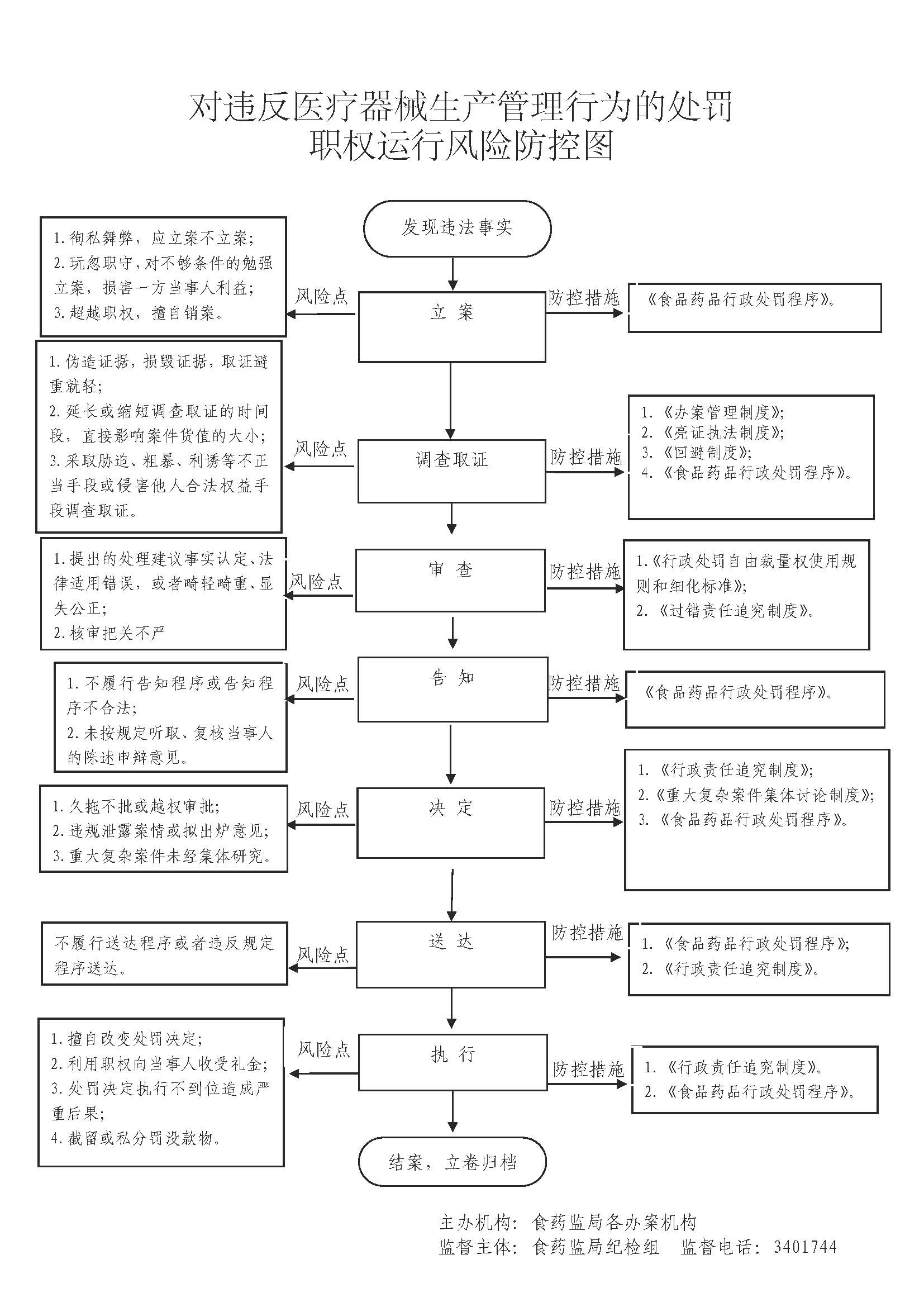
| 行政处罚 | 74602117-4-CF-0049 | 对违反医疗器械生产管理行为的处罚 | 对医疗器械生产企业未按照经注册或者备案的产品技术要求组织生产,或者未依照规定建立质量管理体系并保持有效运行的处罚 | 【行政法规】 《医疗器械监督管理条例》(国务院令第650号)第六十六条第(二)项 【规章】 《医疗器械生产监督管理办法》(2014年国家食品药品监督管理总局令第7号)第六十六条第(二)项 【规章】 《一次性使用无菌医疗器械监督管理办法(暂行)》(2000年国家药品监督管理局令第24号)第十九条、第三十八条 | 1.立案环节责任:在检查中发现或者接到举报有违法行为或者交办、上报、移送的此类违法案件,应予以审查,决定是否立案。 2.调查环节责任:对立案的案件,指定专人负责,与当事人有直接利害关系的应当回避。 3.审查环节责任:应当组织3名以上有关人员对违法行为的事实、性质、情节、社会危害程度、办案程序、处罚意见等进行合议审查。 4.告知环节责任:在做出处罚决定前,应书面告知当事人违法事实、处罚的理由和依据,以及当事人依法享有的陈述、申辩、要求听证等权利。 5.决定环节责任:根据审理情况决定是否予以处罚,对情节复杂或者重大违法行为给予较重的处罚,应当由食品药品监督管理部门负责人集体讨论决定。 6.送达环节责任:处罚决定书应在7日内送达当事人,邮寄送达、公告送达的期限依照《食品药品处罚程序规定》执行。 7.执行环节责任:监督当事人在决定的期限内,履行生效的处罚决定。当事人在法定期限内不申请行政复议或者提起行政诉讼,又不履行的,食品药品监督部门可依法采取加处罚款、查封扣押或向人民法院申请强制执行等措施。 8.其他法律法规规章规定应履行的责任。 | 因不履行或不正确履行行政职责,有下列情形的,行政机关及相关工作人员应承担相应责任: 1.没有法律或者事实依据实施处罚的。 2.指派不具备行政执法资格实施处罚的。 3.擅自设立处罚种类或者改变处罚幅度、范围的。 4.违反法定的处罚程序的。 5.委托不合法主体执法或二次委托执法的。 6.因处罚不当给当事人造成损失的。 7.执法人员玩忽职守,对应当予以制止和处罚的违法行为不予制止、处罚,致使公民、法人或者其他组织的合法权益、公共利益和社会秩序遭受损害的。 8.符合听证条件、行政管理相对人要求听证,应予组织听证而不组织听证的。 9.在处罚过程中发生腐败行为的。 10.处罚不使用罚款、没收财物单据或者使用非法定部门制发的罚款、没收财物单据的。 11.违反规定自行收缴罚款的,向行政机关返还罚款或者拍卖款项的。 12.将罚款、没收的违法所得或者财物截留、私分或者变相私分的。 13.其他违反法律法规规章规定的行为。 | 【法律】 《中华人民共和国行政处罚法》第五十五条、第五十六条、第五十七条、第五十八条、第五十九条、第六十条、第六十一条、第六十二条; 【行政法规】 《医疗器械监督管理条例》(国务院令第650号)第七十四条 【规章】 《山西省行政执法条例》第四十条、第四十一条、第四十二条; | 一、行政处理:诫勉谈话或者责令书面检讨;通报批评;暂扣行政执法证件;责令离岗培训;调离执法岗位,取消执法资格;依法追偿部分或者全部行政赔偿费用。 二、行政处分:警告、记过、记大过、降级、撤职、开除。 三、党纪处分:警告、严重警告、撤销党内职务、留党察看、开除党籍。 四、其他法律责任。 | |
| 对委托不具备规定条件的企业生产医疗器械,或者未对受托方的生产行为进行管理的处罚 | 【行政法规】 《医疗器械监督管理条例》(国务院令第650号)第六十六条第(五)项 【规章】 《医疗器械生产监督管理办法》(2014年国家食品药品监督管理总局令第7号) 第六十六条第(三)项 | ||||||||
| 对医疗器械生产企业的生产条件发生变化、不再符合医疗器械质量管理体系要求,未依照规定整改、停止生产、报告的处罚 | 【行政法规】 《医疗器械监督管理条例》(国务院令第650号)第六十七条第(一)项 【规章】 《医疗器械生产监督管理办法》(2014年国家食第六十七条 | ||||||||
| 对医疗器械生产企业未按照要求提交质量管理体系自查报告的处罚 | 【行政法规】 《医疗器械监督管理条例》(国务院令第650号) 第六十八条第(一)项 【规章】 《医疗器械生产监督管理办法》(2014年国家食品药品监督管理总局令第7号)第六十八条 | ||||||||
| 对出厂医疗器械未按照规定进行检验的处罚 对出厂医疗器械未按照规定附有合格证明文件的处罚 对医疗器械产品连续停产一年以上且无同类产品在产,未经所在地省、自治区、直辖市或者设区的市级食品药品监督管理部门核查符合要求即恢复生产的处罚 对向监督检查的食品药品监督管理部门隐瞒有关情况、提供虚假资料或者拒绝提供反映其活动的真实资料的处罚 | 【规章】 《医疗器械生产监督管理办法》(2014年国家食品药品监督管理总局令第7号) 第六十九条第(一)项、第六十九条第(二)项、第六十九条第(五)项、第六十九条第(六)项 | ||||||||